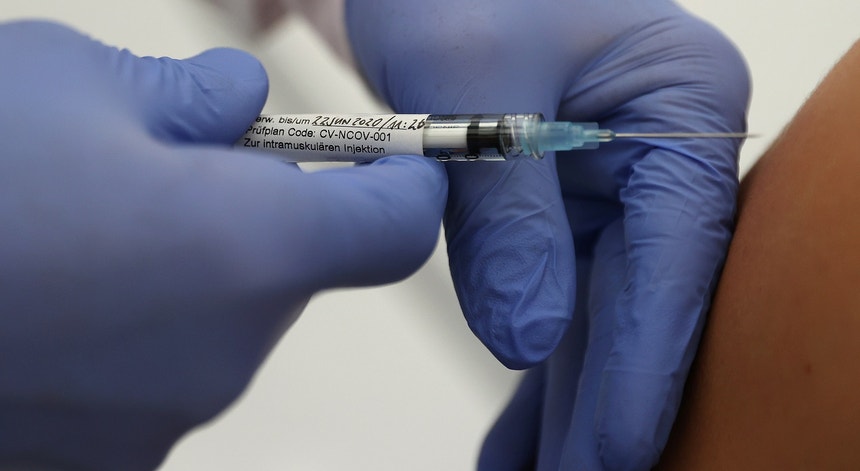
A vacina que está a ser produzida pela empresa de biotecnologia Moderna conseguiu gerar anticorpos em todas as pessoas que participaram nos testes e mostra resultados promissores com muito poucos efeitos secundários. O epidemiologista Anthony Fauci chama aos resultados provisórios "muito boas notícias”.
Os resultados publicados na terça-feira confirmam que todos os indivíduos que participaram nos testes desenvolveram proteção contra a doença sem efeitos secundários significativos. "Esta é uma notícia muito boa", disse o diretor Instituto Nacional de Alergias e Doenças Infecciosas, Athony Fauci ao Wall Stret Journal.
Todos os 45 participantes, dos 18 aos 55 anos, desenvolveram anticorpos neutralizantes ao vírus com níveis similares aos registados em pessoas que recuperaram naturalmente da covid-19.
A vacina da Moderna foi a primeira a entrar em testes clínico, de um total de 23 a nível mundial.
"Os anticorpos neutralizantes são a coisa mais importante na proteção contra uma infeção viral", disse Fauci. "Os dados do estudo - embora os números sejam pequenos - tornam muito claro que esta vacina é capaz de induzir níveis muito bons de anticorpos neutralizantes”.
Os dados dos ensaios da fase 1 "mostram que a vacinação com mRNA-1273 (o nome da vacina candidata) provoca uma resposta imunitária a todos os níveis de dose", disse o diretor médico de Moderna, Tal Zanks e não demonstraram qualquer restrição de segurança com mais do que uma inoculação, a opção que deverá ser testada na próxima fase.
Os efeitos secundários mais frequentemente notificados após a segunda vacinação na dose de 100-microgramas foram a fadiga, entre 80%; arrepios (80%); dores de cabeça (60%); e mialgia ou dores musculares, entre 53%. Foram todos transitórios e de gravidade ligeira ou moderada, tal como referido no comunicado de imprensa do Moderna.
O governo dos EUA apoiou a investigação com quase 500 milhões de dólares.
“As respostas imunitárias parecem promissoras, mas não sabemos ainda que os níveis que estamos a ver vai proteger de facto contra a infeção. É realmente difícil saber isso até que se faça o teste de eficácia”, revelou a Dra Lisa Jackson, uma investigadora no Kaiser Permanente Washington Health Research Institute, que esteve envolvida no estudo.O estudo passa agora para a Fase 3, que terá início a 27 de Julho com 30 mil participantes em 87 locais diferentes nos Estados Unidos. É o último passo antes dos reguladores decidirem se pode ser comercializada.
Os investigadores irão administrar a vacina a metade dos participantes e um placebo à outra metade. O estudo está previsto para durar até outubro de 2022, embora os resultados possam ser conhecidos antes dessa data.
“Esperamos com expetativa o início da fase 3 da mRNA-1273 para demonstrar que a capacidade da nossa vacina para reduzir o risco de contrair a covid-19”, acrescentou o responsável.
“O que é que nós queremos saber? Se a vacina é segura e eficaz. É isso que queremos saber”, diz o Dr. Paul Offit, membro do painel da NIH que desenhou as diretrizes para os estudos das vacinas e que não está envolvido no estudo.
Com o estudo já feito, “sabemos que é segura para 45 pessoas, mas será para 20 milhões ou 200 milhões?”, acrescenta Offit.
A Fase 1 testa um pequeno número de pessoas e foca-se em saber se a vacina é segura e se gera uma resposta imunitária. A Fase 2 faz uma expansão do alvo do estudo e é dada a pessoas com características idênticas às da população a quem se destina a vacina. Na Fase 3, a vacina é dada a milhares de pessoas e é testada de novo a eficácia e segurança.


