Mundo
COVID-19
Covid-19. Pressa de conseguir um medicamento pode viciar a investigação
Algumas das normas científicas poderão a estar a ser desrespeitadas para responder à urgência na busca de tratamento para a Covid-19. O uso de Remdesivir – um dos medicamentos mais promissores – já foi autorizado para alguns dos doentes mais graves nos EUA. Especialistas defendem, no entanto, que esta autorização teve como base estudos que são ainda preliminares e não acreditam realmente no benefício deste fármaco.
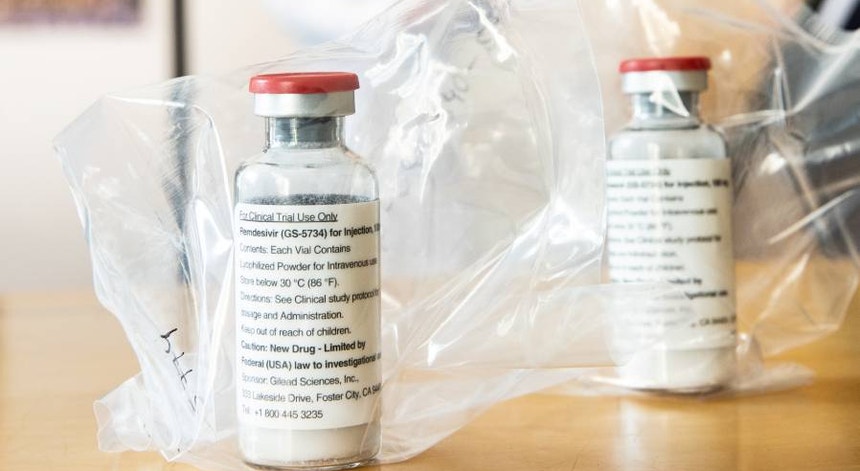
Dada a complexidade do desenvolvimento de uma vacina que cure a infeção por Covid-19, a prioridade tem estado centrada em possíveis tratamentos que possam melhorar e acelerar a recuperação.
O Remdesivir - medicamnto usado para tratar doenças como Ébola e Síndrome Respiratória do Médio Oriente (MERS) - é um dos tratamentos mais promissores contra a Covid-19, para além dos antimaláricos cloroquina e hidroxicloroquina.
Este anseio pela rápida busca de um tratamento para o novo coronavírus poderá estar, no entanto, a prejudicar os métodos científicos e as opiniões sobre os benefícios do Remdesivir são contraditórias.
Os padrões científicos exigem que os resultados sejam revistos por especialistas independentes e os ensaios devem ter como base um número significativo de pacientes, bem como um grupo de controlo que determine a fiabilidade do estudo. Se tivermos estes critérios como base, ainda não existem dados que comprovem que o medicamento Remdesivir traz benefícios na recuperação da infeção por Covid-19, apesar de a farmacêutica responsável pela produção do fármaco, Gilead Sciences, garantir o contrário.
Um estudo clínico desenvolvido na China sobre o estudo deste fármaco para o tratamento da Covid-19 analisou 237 pacientes e previa que, se o medicamento fosse administrado aos pacientes ainda numa fase inicial da infeção, estes poderiam apresentar melhorias na recuperação e no prognóstico. No entanto, o estudo concluiu que “o tratamento com remdesivir não acelera a cicatrização nem reduz a mortalidade da covid-19, em comparação com o placebo”.
Na passada quinta-feira, a farmacêutica norte-americana anunciou a obtenção de resultados aparentemente positivos sobre o seu antiviral com base num ensaio clínico conduzido pelo Instituto Nacional de Alergias e Doenças Infeciosas que estudou mais de mil pacientes gravemente infetados com Covid-19. De acordo com este estudo, o tempo de recuperação com Remdesivir diminui de 15 para 11 dias.
Porém, tal como ressalva o jornal espanhol El País, também estes dados levantam dúvidas do ponto de vista científico, uma vez que não foram ainda revistos por especialistas independentes e o estudo não incluiu um grupo de inspeção para determinar se a melhoria observada foi derivada, ou não, do medicamento. Na sequência destes resultados positivos, a Administração Federal de Alimentos e Medicamentos dos Estados Unidos (FDA) emitiu na sexta-feira uma autorização de emergência para o fármaco Remdesivir. No domingo, a Gilead Sciences anunciou que o medicamento antiviral injetável estará disponível na próxima semana para alguns dos doentes de Covid-19 mais graves nos Estados Unidos.
"Como parte do compromisso da FDA em acelerar o desenvolvimento e a disponibilidade de possíveis tratamentos para a Covid-19, a agência tem estado envolvida em discussões com a Gilead Sciences a respeito da disponibilização do Remdesivir aos pacientes o mais rápido possível, conforme apropriado", revelou o porta-voz da FDA, Michael Felberbaum.
Apesar de ainda não existirem dados que comprovem a eficácia e segurança do uso de Remdesivir, a Gilead Sciences já anunciou que multiplicou a sua capacidade de produção do fármaco e o objetivo é produzir um milhão até ao final do ano.
Por enquanto, todos os dados têm como base doentes graves e hospitalizados. Prevê-se que no final deste mês, a Gilead Sciences fornecerá os dados referentes aos seus testes sobre infeções menos graves.
“Os benefícios não me convencem”
Os dados que têm vindo a surgir sobre os benefícios do Remdesivir suscitam, por isso, dúvidas por parte dos especialistas.
“Os benefícios não me convencem”, disse a El País Julián Pérez- Villacastín, médico do Hospital Clínico de Madrid e presidente da Sociedade Espanhola de Cardiologia (SEC). “Para um medicamento tão caro, porque é de esperar que o seja, exigimos que reduza a mortalidade, que os pacientes vivam mais e melhor, o que, por enquanto, não foi comprovado”, acrescentou.
“A verdade será conhecida no final, mas não há necessidade de pressas. Anúncios como os que temos visto servem apenas para gerar preocupação e há pessoas que tentam obtê-lo por meios legais e ilegais. Os únicos que saem a ganhar são os produtores do medicamento”, sublinha Pérez-Villacastín.
Antoni Trilla, epidemiologista e consultor científico do governo espanhol, defende que “estes são resultados preliminares que terão de ser revistos para perceber em quais dos pacientes foi aplicado [o Remdesivir] com sucesso e em que fase da doença se apresentam (...) É aconselhável esperar por novos estudos que confirmem ou infirmem o que foi observado e só então se decida se o seu uso sistemático é justificado”, sublinhou Trilla.
O Remdesivir - medicamnto usado para tratar doenças como Ébola e Síndrome Respiratória do Médio Oriente (MERS) - é um dos tratamentos mais promissores contra a Covid-19, para além dos antimaláricos cloroquina e hidroxicloroquina.
Este anseio pela rápida busca de um tratamento para o novo coronavírus poderá estar, no entanto, a prejudicar os métodos científicos e as opiniões sobre os benefícios do Remdesivir são contraditórias.
Os padrões científicos exigem que os resultados sejam revistos por especialistas independentes e os ensaios devem ter como base um número significativo de pacientes, bem como um grupo de controlo que determine a fiabilidade do estudo. Se tivermos estes critérios como base, ainda não existem dados que comprovem que o medicamento Remdesivir traz benefícios na recuperação da infeção por Covid-19, apesar de a farmacêutica responsável pela produção do fármaco, Gilead Sciences, garantir o contrário.
Um estudo clínico desenvolvido na China sobre o estudo deste fármaco para o tratamento da Covid-19 analisou 237 pacientes e previa que, se o medicamento fosse administrado aos pacientes ainda numa fase inicial da infeção, estes poderiam apresentar melhorias na recuperação e no prognóstico. No entanto, o estudo concluiu que “o tratamento com remdesivir não acelera a cicatrização nem reduz a mortalidade da covid-19, em comparação com o placebo”.
Numa declaração, Gilead lamentou os dados publicados, “uma vez que o estudo, devido à baixa amostra, foi insuficiente para permitir conclusões estatisticamente significativas. Como tal, os resultados são inconclusivos”.
Na passada quinta-feira, a farmacêutica norte-americana anunciou a obtenção de resultados aparentemente positivos sobre o seu antiviral com base num ensaio clínico conduzido pelo Instituto Nacional de Alergias e Doenças Infeciosas que estudou mais de mil pacientes gravemente infetados com Covid-19. De acordo com este estudo, o tempo de recuperação com Remdesivir diminui de 15 para 11 dias.
Porém, tal como ressalva o jornal espanhol El País, também estes dados levantam dúvidas do ponto de vista científico, uma vez que não foram ainda revistos por especialistas independentes e o estudo não incluiu um grupo de inspeção para determinar se a melhoria observada foi derivada, ou não, do medicamento. Na sequência destes resultados positivos, a Administração Federal de Alimentos e Medicamentos dos Estados Unidos (FDA) emitiu na sexta-feira uma autorização de emergência para o fármaco Remdesivir. No domingo, a Gilead Sciences anunciou que o medicamento antiviral injetável estará disponível na próxima semana para alguns dos doentes de Covid-19 mais graves nos Estados Unidos.
"Como parte do compromisso da FDA em acelerar o desenvolvimento e a disponibilidade de possíveis tratamentos para a Covid-19, a agência tem estado envolvida em discussões com a Gilead Sciences a respeito da disponibilização do Remdesivir aos pacientes o mais rápido possível, conforme apropriado", revelou o porta-voz da FDA, Michael Felberbaum.
Apesar de ainda não existirem dados que comprovem a eficácia e segurança do uso de Remdesivir, a Gilead Sciences já anunciou que multiplicou a sua capacidade de produção do fármaco e o objetivo é produzir um milhão até ao final do ano.
Por enquanto, todos os dados têm como base doentes graves e hospitalizados. Prevê-se que no final deste mês, a Gilead Sciences fornecerá os dados referentes aos seus testes sobre infeções menos graves.
“Os benefícios não me convencem”
Os dados que têm vindo a surgir sobre os benefícios do Remdesivir suscitam, por isso, dúvidas por parte dos especialistas.
“Os benefícios não me convencem”, disse a El País Julián Pérez- Villacastín, médico do Hospital Clínico de Madrid e presidente da Sociedade Espanhola de Cardiologia (SEC). “Para um medicamento tão caro, porque é de esperar que o seja, exigimos que reduza a mortalidade, que os pacientes vivam mais e melhor, o que, por enquanto, não foi comprovado”, acrescentou.
“A verdade será conhecida no final, mas não há necessidade de pressas. Anúncios como os que temos visto servem apenas para gerar preocupação e há pessoas que tentam obtê-lo por meios legais e ilegais. Os únicos que saem a ganhar são os produtores do medicamento”, sublinha Pérez-Villacastín.
Antoni Trilla, epidemiologista e consultor científico do governo espanhol, defende que “estes são resultados preliminares que terão de ser revistos para perceber em quais dos pacientes foi aplicado [o Remdesivir] com sucesso e em que fase da doença se apresentam (...) É aconselhável esperar por novos estudos que confirmem ou infirmem o que foi observado e só então se decida se o seu uso sistemático é justificado”, sublinhou Trilla.
